عصوية جمرية
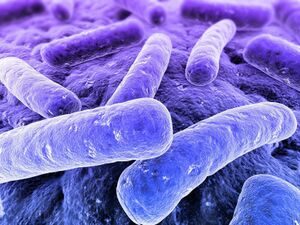
العصوية الجمرية العصية الجمرية B. anthracis هي عصية هوائية كبيرة مكونة للأبواغ إيجابية الغرام، تنمو جيداً على وسائط الزرع المعروفة مثل الأغار الدموي. وتبدو العصية الجمرية الملونة المأخوذة من وسائط الزرع على شكل سلاسل طويلة متشابهة من العضويات ذات النهايات المربعة مما يجعلها تشبه الشاحنات الصندوقية boxcars.
| عصوية جمرية | |
|---|---|
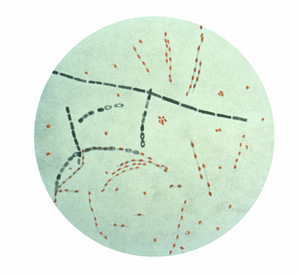
| |
| Photomicrograph of Bacillus anthracis, stained using fuchsin-methylene blue spore stain) | |
| التصنيف العلمي | |
| أصنوفة غير معروفة (أصلحها): | Bacillus |
| Species: | Template:Taxonomy/BacillusB. anthracis
|
| Binomial name | |
| Template:Taxonomy/BacillusBacillus anthracis Cohn 1872
| |
يمكن أن تبقى أبواغ الجمرة الخبيثة عيوشة viable ومعدية لعدة سنوات وحتى عقود في التربة، وتكون أثناء هذه الفترة مصدراً محتملاً لخمج المواشي آكلة العشب، لكنها لا تمثل بشكل عام خطراً خمجياً مباشراً على الإنسان. قد تصبح الحيوانات مخموجة عندما تأكل الأبواغ أو تستنشقها أثناء رعيها. أما الإنسان فقد يصبح مخموجاً بالعصية الجمرية عن طريق التماس الجلدي أو ابتلاع أو استنشاق أبواغ العصية الجمرية التي مصدرها منتجات الحيوانات المصابة أو عن طريق استنشاق الأبواغ من البيئة المحيطية.
يمكن أن تتعطل الأبواغ بالتماس لمدة كافية مع بخار البارافورمالدهید paraformaldehyde أو مع الهيبوكلورايت 5% (% 5 hypochlorite) أو مع محلول الفينول phenol أو باستعمال جهاز التعقيم بالبخار (الموصدة autoclaving).
تنتش ابواغ الجمرة الخبيثة عندما تصل لبيئة غنية بالحموض الأمينية والنيوكلوزيدات nucleosides والغلوكوز مثل دماء وأنسجة الحيوانات. ويؤدي تنسخ الجراثيم لإنتاج ثلاثة بروتينات:
- المستضد الوافي protective antigen) PA).
- العامل المميت lethal factor) LF).
- العامل المودم edema factor) EF).
تتحد هذه البروتينات لتشكل ذيفانين هما الذيفان المميت والذيفان الموذم. حيث يشكل PA وLF الذيفان المميت، وهو بروتياز protease يعتقد أنه مسؤول عن تخرب الأنسجة والصدمة والوفاة، لكن آلية ذلك غير واضحة. بينما يشكل PA وEF الذيفان الموذم، وهو محلقة الأدينيلات adenylate cyclase وتؤدي لخلل في السيطرة على مرور الشوارد والماء عبر أغشية الخلايا مما يؤدي لوذمة شاملة.
يرتبط PA مع مستقبلات موجودة على خلايا الثديات، ثم يرتبط مع LF أو EF. تدمج المعقدات الذيفانية بالجسيم الداخلي endosome للخلية، ثم تنتقل إلى العصارة الخلوية cytosol حيث تفعل فعلها هناك على الأقل.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الجمرة الخبيثة
مرض حيواني المصدر Zoonotic disease ناجم عن جراثيم مكونة للأبواغ هي العصية الجمرية Bacillus anthracis. قدر عدد الوفيات عند البشر الناجمة عن وباء الجمرة الخبيثة الذي حدث في أوروبا في القرن السابع عشر 60,000 حالة وفاة. وقد عرفت الطبيعة المعدية للجمرة الخبيثة في عام 1823.
التسمية
اشتق تعبير Anthrax من الكلمة الإغريقية anthrakis التي تعني الفحم؛ وذلك بسبب الآفات الجلدية السوداء المميزة لهذا المرض.
التاريخ
وصف أحد الأمراض (الذي يبدو أنه كان مرض الجمرة الخبيثة) عام 1490 قبل الميلاد في سفر الخروج في العهد القديم وأطلق عليه اسم الطاعون الخامس. كما عثر على كتابات هندية وإغريقية قديمة تصف إصابة الناس والحيوانات بالجمرة الخبيثة.
وصفت العصية الجمرية لأول مرة في عام 1849، وكان روبرت كوخ Robert Koch أول من أكد المنشأ الجرثومي لهذا المرض في عام 1876. تم تطوير وتجربة أول لقاح حيواني مضعف من قبل لويس باستور Luis Pasteur في عام 1881. وفي عام 1939 تم تكوين لقاح حيواني محسن يحتوي معلقاً من سلالة حية للعصية الجمرية عديمة الفوعة وغير ممحفظة. و تمت الإشارة إلى دور الذيفان toxin في إمراض الجمرة الخبيثة في عام 1954. أما اللقاح البشري المؤلف من رشاحة زرعية لا خلوية فتم تطويره في عام 1954. بينما تم ترخيص العمل بلقاح محسن لا خلوي في الولايات المتحدة في عام 1970. وتم استعمال الجمرة الخبيثة كسلاح بيولوجي بفعالية لأول مرة في عام 2001.
الإمراض
بعد تلقيح inoculation الجروح بأبواغ العصية الجمرية أو بعد ابتلاعها تقوم البالعات الكبيرة بابتلاع هذه الأبواغ، حيث تنتش فيها. وتقوم الجراثيم الإنباتية vegetative بإنتاج محفظة تسمح لها بتجنب الجهاز المناعي من خلال مقاومة البلعمة وحماية الجراثيم من الانحلال بالبروتينات الهابطية cationic في المصل. كما يتم إنتاج الذيفان المميت والذيفان الموذم، فإذا لم يتم احتواء الجراثيم فيمكنها أن تنتشر إلى العقد اللمفية النازحة وإلى المسافة داخل الخلوية intracellular مما يؤدي لإنتاج الذيفانات الأخرى. وتؤدي الذيفانات إلى نخر النسيج اللمفي مما يؤدي لتحرر أعداد كبيرة من الجراثيم، وقد يتلو ذلك تجرثم الدم، مما يؤدي لحدوث إنتان دم ساحق overwhelming وتخرب نسجي شامل وقصور الأعضاء والوفاة.
تنتقل الأبواغ في الجمرة الخبيثة الاستنشاقية من الأسناخ إلى العقد اللمفية الرغامية القصبية والعقد اللمفية المنصفية. ويؤدي إنتاج الذيفان المميت والذيفان الموذم لنخر نسجي ووذمة شاملة.
كما يؤدي إنتاج الذيفانات إلى التهاب عقد لمفية نزفية شديد massive hemorrhagic lymphadenitis، والتهاب منصف mediastinitis مميز للمرض الاستنشاقي.
تشير الدراسات على الحيوانات إلى أن الأبواغ المستنشقة قد لا تتش مباشرة في الأسناخ بل تبقى كامنة فيها لعدة أسابيع وربما أشهر حتى تبتلع من قبل البالعات السنخية الكبيرة، عندها تأخذ الأبواغ بالإنتاش وتبدأ بالتنسخ في البالعات الكبيرة وفي النسيج اللمفي.
إن المضادات الحيوية فعالة ضد عصيات الجمرة المنتشة أو الإنباتية، بينما ليست فعالة ضد الأشكال اللاإنباتية أو البوغية للجرثومة. لذلك يمكن منع تطور المرض طالما تتم المحافظة على مستوی علاجي للمضادات الحيوية كاف لقتل جراثيم الجمرة الخبيثة. أما بعد إيقاف المضادات الحيوية فيتطور المرض إذا كانت أعداد الأبواغ غير المنتشة المتبقية كافية لتجنب الجهاز المناعي أو التغلب عليه عندما تنتش. إن هذه الظاهرة من تأخر بدء المرض لا يعرف حدوثها عند التعرض الجلدي أو الهضمي.
الأعراض السريرية
تتحدد اعراض الجمرة الخبيثة عند الإنسان وطور حضانتها بطريق انتقال الجرثومة. وهناك ثلاثة أشكال سريرية للجمرة الخبيثة هي:
- الجمرة الجلدية.
- الجمرة الهضمية.
- الجمرة الاستنشاقية.
الجمرة الخبيثة الجلدية
تحدث معظم إصابات العصية الجمرية (أكثر من 95%) في الحالة الطبيعية عن طريق الجلد. وتحدث عندما تدخل الجرثومة من خلال جرح جلدي أو سحجة جلدية (مثلاً عند التعامل مع الحيوانات الملوثة بالعصية الجمرية أو مع منتجاتها أو مع أشياء أخرى).
يتراوح طور حضانة الجمرة الخبيثة الجلدية المسجلة بين 0.5 - 12 يوماً. ويبدأ الخمج الجلدي بشكل حطاطة صغيرة قد تكون حاكة، ثم تتطور لحويصل خلال يوم ليومين، ثم تتآكل مخلفة قرحة نخرية (خشکریشة eschar) ذات مركز أسود مميز. وقد تتطور حويصلات ثانوية حول الآفات الأولية، وتكون الآفة عادة غير مؤلمة.
يمكن أن تشمل الأعراض الأخرى تورم العقد اللمفية المجاورة والحمى والدعث والصداع. يقترح تشخيص الجمرة الخبيثة الجلدية بوجود خشکريشة ووذمة غير متناسبة مع حجم الآفة وانعدام الألم خلال الأطوار البدئية للخمج.
يتراوح معدل إماتة الحالات في الجمرة الخبيثة الجلدية بين 5% - 20٪ في حال عدم استعمال المعالجة بالمضادات الحيوية، بينما يكون هذا المعدل أقل من 1٪ في حال المعالجة بالمضادات الحيوية.
الجمرة الخبيثة الهضمية
غالباً ما يحدث الشكل المعوي للجمرة الخبيثة بعد تناول اللحم الملوث. ويعتقد أن دور الحضانة يتراوح بين 1-7 أيام. تتميز إصابة البلعوم بآفات على قاعدة اللسان أو اللوزتين مع التهاب بلعوم وعسرة بلع وحمى واعتلال عقد لمفية موضعية. أما إصابة الأمعاء السفلية فتتميز بالتهاب حاد في الأمعاء، وتتألف العلامات البدئية من غثيان ونقص شهية وإقياء وحمى، يتلوها ألم بطني واقياء دموي وإسهال مدمی. إن معدل إماتة الحالات في الجمرة الخبيثة الهضمية غير معروف، لكنه يقدر بحوالي 25٪ - 60٪.
الجمرة الخبيثة الاستنشاقية
تعرف الجمرة الخبيثة الاستشاقية في الأصل بمرض فارزي الصوف woolsorter، وهي تنجم عن استنشاق 8.000 - 50.000 بوغ من أبواغ العصية الجمرية. يعتقد أن هذا الشكل من الجمرة الخبيثة هو الأكثر شيوعاً بعد إطلاق العصية الجمرية المتعمد. وتتراوح فترة حضانة الجمرة الخبيثة الاستنشاقية عند الإنسان بين 1-7 أيام، وقد تمتد لمدة 43 يوماً.
أما فترة الحضانة الوسطية للحالات العشر الأولى من الجمرة الخبيثة الاستشاقية المرتبطة بالإرهاب البيولوجي الذي حدث عام 2001 فكانت 4 أيام وبمجال تراوح بين 4 - 6 أيام. قد تتناسب فترة حضانة الجمرة الخبيثة الاستنشاقية عكسياً مع جرعة العصيات الجمرية.
تقترح معطيات الدراسات المخبرية المجراة على الحيوانات استمرار إنتاش أبواغ العصيات الجمرية في المضيف لعدة أسابيع بعد الاستنشاق، و أن المضادات الحيوية قد تطيل فترة المرض المتطور. يمكن أن تتضمن الأعراض البدئية للجمرة الخبيثة الاستنشاقية السعال غير المنتج والألم العضلي والتعب والحمى، و كان التعرق الغزير الذي يبلل المريض هو العرض المسيطر غالباً في الحالات العشر الأولى المرتبطة بالهجوم البيولوجي في عام 2001. لقد سجل حدوث فترة قصيرة من التحسن تالية للأعراض البادرية prodromal، لكنها لم تشاهد في الحالات التي حدثت في عام 2001. ثم يحدث تدهور سريع بالأعراض مع حمى شديدة وعسرة تنفسية وزرقة وصدمة.
غالبا ما تظهر صورة الصدر وجود انصباب جنبي واتساع المنصف الناجم عن اعتلال العقد اللمفية. يحدث التهاب السحايا عند نسبة تصل إلى 50% من المرضى المصابين بالجمرة الخبيثة الاستنشاقية، وغالباً ما يكون نزفياً.
كان معدل إماتة الحالات قبل الهجمات البيولوجية عام 2001 يتراوح بين 85٪ - 97% في حال عدم استعمال المضادات الحيوية، بينما قدر بحوالي 75% في حال استعمال المضادات الحيوية. أما حالات الجمرة الخبيثة الاستنشاقية التي حدثت في عام 2001، فكان معدل إماتة الحالات فيها مع المعالجة المركزة 745 (5 وفيات من أصل 11 حالة). تحدث الوفاة في بعض الأحيان خلال ساعات من بداية المرض.
قد تكون الأعراض الباكرة للجمرة الخبيثة الاستنشاقية مشابهة للأعراض الأولية للمرض الشبيه بالإنفلونزا influenza - like illness) LI)، وهو مرض تنفسي لا نوعي، يتميز بالتعب والحمى والسعال وأعراض أخرى. ومعظم حالات ILI لا تنجم عن الإنفلونزا بل عن ڤيروسات أخرى مثل الڤيروسات الأنفية rhinovirus والڤيروسات الغدية adenovirus. إن الاحتقان الأنفي والسيلان الأنفي شائعان عند الإصابة بـ ILI لكنهما غير شائعين عند الإصابة بالجمرة الخبيثة الاستنشاقية، بينما يكون ضيق النفس شائعاً في الإصابة بالجمرة الخبيثة الاستنشاقية وغير شائع في ILI.
إن معظم الأشخاص المصابين بالجمرة الخبيثة الاستنشاقية لديهم شذوذات في صورة الصدر الشعاعية، في حين لا يكون لدى معظم المصابين بـ ILI أي شذوذات في صورة الصدر (رغم أن المصابين بالإنفلونزا قد يحدث عندهم ذات رئة بدئية بالإنفلونزا أو ذات رئة جرثومية ثانوية).
التشخيص المخبري
يجب الاشتباه بتشخيص الجمرة الخبيثة الجلدية عند وجود القرحة الضحلة غير المؤلمة المميزة مع الجلبة crust السوداء. يظهر تلوين غرام للسائل الحويصلي جراثيم نموذجية إيجابية الغرام، ويمكن تأكيد التشخيص بالزرع.
أما الجمرة الخبيثة الهضمية فتكون صعبة التشخيص؛ نظراً لتشابهها مع الأمراض الهضمية الشديدة الأخرى. وقد يساعد على التشخيص وجود قصة تناول لحم يحتمل أن يكون ملوثاً مع وجود أعراض نموذجية.
كذلك فقد يكون تشخيص الجمرة الخبيثة الاستنشاقية صعباً، ويشكل اتساع المنصف على صورة الصدر الشعاعية علامة سريرية مساعدة على وضع التشخيص. قد يكون الحمل الجرثومي , bacterial burden في الخمج المتقدم كبيراً جداً بحيث تشاهد الجراثيم باستعمال تلوين غرام على الدم المحيطي غير المثفل unspun. يمكن أن توجد جراثی إيجابية الغرام في عينات سريرية أخرى مثل السائل الجنبي أو الخزعة الجلدية من منطقة الإصابة أو قرحات البلعوم الفموي أو السائل الدماغي الشوكي. يتم تأكيد التشخيص غالباً بإيجابية زرع العصية الجمرية. ويجب أن تظهر زروع الدم القياسية نمواً جرثومياً خلال 6 - 24 ساعة.
يمكن للاختبارات المخبرية الأخرى أن تساعد على وضع التشخيص مثل تفاعل سلسلة البوليميراز polymerase chain reaction) PCR) الذي يكشف DNA العصية الجمرية في السائل الجنبي أو الدم والفحوص المصلية PA- based ELISA والكيمياء الهيستولوجية المناعية النسجية tissue immunohistochemistry التي يتم فيها تلوين النسيج بأضداد نوعية لجدار الخلية وللمحفظة.
التدبير الطبي
تعتبر المضادات الحيوية المداخلة العلاجية الأكثر أهمية في أي شكل من أشكال الجمرة الخبيثة، ويجب البدء بها مباشرة عند الاشتباه بالمرض. وتعتبر سلالات العصية الجمرية التي تحدث بشكل طبيعي حساسة بشكل نموذجي للعديد من المضادات الحيوية والتي تشمل البنسلين، والتتراسيكلين والفلوروکینولونات الفموية (السيبروفلوكساسين ciprofloxacin والأفلوكساسين .(ofloxacin
تنتج العصيات الجمرية السيفالوسبوريناز cephalosporinase التي تثبط تأثير السيفالوسبورينات المضاد للجراثيم مثل السيفترياكسون ceftriaxone، لذلك يجب عدم استعمال السيفالوسبورينات في معالجة الجمرة الخبيثة. كذلك فإن سلالات العصية الجمرية التي تحدث بشكل طبيعي قد تكون مقاومة للمضادات الحيوية شائعة الاستعمال مثل السلفاميثوكسازول sulfamethoxazole والتريميتوبریم trimethoprim والأزتریونام aztreonam.
كانت نسبة البقيا survival عند المصابين بالجمرة الخبيئة الاستنشاقية المرتبطة بالهجوم البيولوجي عام 2001 أعلى (55 %) من نسبة البقيا المذكورة سابقاً. وقد أعطي كل المرضى علاجاً مشتركاً بالمضادات الحيوية حيث استخدم اكثر من مضاد حيوي فعال ضد عصيات الجمرة. إن التحسن الواضح في نسبة البقيا يشير إلى أن المضادات الحيوية المشتركة المستعملة عند هؤلاء المرضى قد يكون لها أفضلية علاجية مقارنة مع النظم العلاجية السابقة. وتقترح معطيات محدودة في المعالجة أن المعالجة الوريدية الباكرة بالفلوروكينولونات (مثل السيبروفلوكساسين) مع واحد على الأقل من الأدوية الأخرى الفعالة (مثل الريفامبين، الفانكوميسين، البنسلين، الأمبيسلين، الكلورامفينيكول، الكلينداميسين) قد تحسن البقيا.
يجب البدء بالمعالجة الوريدية، ومن ثم تعطی معالجة فموية عندما تصبح الحالة السريرية مناسبة. كذلك يجب الاستمرار باستخدام المضادات الحيوية لمدة 30 - 60 يوماً أو أكثر.
يبدو أن نسبة البقيا عند المصابين بالجمرة الخبيثة الاستنشاقية تزداد باللجوء للعناية الداعمة الهجومية aggressive مثل نزح الانصبابات الجنبية و تصحيح اضطراب الشوارد والاضطراب الحامضي القلوي واستعمال التهوية الآلية باكراً، وذلك بالإضافة لاستعمال المضادات الحيوية.
يوصى باستعمال السيبروفلوكساسين أو الدوكسي سيكلين doxycycline كخط علاجي أول عند الإصابة بالجمرة الخبيثة الجلدية. كما يوصى بالمعالجة الوريدية بالنظام متعدد الأدوية في الجمرة الخبيثة الجلدية مع وجود علامات جهازية أو في حال الوذمة الشاملة أو في الآفات التي تصيب الوجه أو العنق. تعالج الجمرة الخبيثة الجلدية بشكل نموذجي لمدة 7 - 10 أيام، لكن في حالة الهجوم البيولوجي قد يكون خطر التعرض الضبوبي aerosol (الاستنشاق) العفوي عاليا؛ لذلك يجب أن تتم معالجة المصابين بالجمرة الخبيثة الجلدية المرافقة لهجوم بيولوجي لمدة 60 يوماً. تجدر الإشارة إلى إن الجمرة الخبيثة الجلدية تستمر بالتطور حتى مرحلة الخشكريشة رغم المعالجة السريعة بالمضادات الحيوية المناسبة.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
الوبائيات
- الحدوث: تحدث الجمرة الخبيثة في جميع أنحاء العالم، وتكون أكثر شيوعاً في المناطق الزراعية التي تفتقر لبرامج سيطرة كافية على الجمرة الخبيثة عند المواشي. تشمل هذه المناطق أمريكا الجنوبية والوسطى وأوروبا الجنوبية والشرقية وافريقيا وآسيا ومنطقة البحر الكاريبي والشرق الأوسط. لقد كانت الجمرة الخبيثة نادرة جداً في الولايات المتحدة قبل عام 2001 ولم يكن هناك حالات مسجلة عند البشر بين عامي 1993 - 2000.
- المستودع: إن المستودعين الرئيسين للجمرة الخبيثة هما الحيوانات المصابة والتربة. وإن أبواغ الجمرة الخبيثة مقاومة بشدة للعوامل الفيزيائية والكيماوية، وتبقى حية في البيئة المحيطية عدة سنوات، ويمكنها أن تبقى هاجعة في بعض أنماط التربة لعدة عقود.
الانتقال
إن الطريقة الأشيع لانتقال الجمرة الخبيثة هي التماس المباشر مع الحيوان المصاب. ويمكن للعصية الجمرية أن تدخل الجسم من خلال آفة جلدية موجودة سابقاً، كما يمكنها أن تدخل بشكل غير مقصود عن طريق الأذية بأداة ملوثة وتكون النتيجة في هذه الحالة حدوث الجمرة الخبيثة الجلدية. وفي بعض الظروف يمكن للنواقل vectors مثل الذباب والنسور أن تنشر جراثيم الجمرة بشكل آلي، لكن لا يعتقد أن للنواقل دوراً هاماً في خمج الإنسان. كما يمكن أن تنتقل عصيات الجمرة الخبيثة عن طريق لحوم الحيوانات المصابة إذا ما تم تناولها دون طهي جيد.
قد تنتقل العصية الجمرية أيضاً عن طريق استنشاق الأبواغ المحمولة بالهواء أو الأبواغ الموجودة بشكل ضبوبي. يبلغ قطر أبواغ العصية الجمرية في الطبيعة 2 - 6 میکرون، وإذا انتشرت في الهواء بشكل ضبوبي نتيجة إجراء عمليات معالجة صناعية للمنتجات الحيوانية الملوثة أو نتيجة هجوم بيولوجي فإن الجزيئات التي يزيد قطرها عن 5 میکرون تسقط بسرعة من الجو وتعلق على أي سطح. ويصبح من الصعب تعليقها في الهواء ثانية، لكنها يمكن أن تبقى في البيئة عدة سنوات. أما الأبواغ ذات الأقطار بين 2 - 5 میکرون فتسلك سلوك الغاز، وتتحرك في البيئة بدون استقرار، ويمكنها أن تعبر مسام الورق كما حدث في المرافق البريدية بعد هجمات الجمرة في عام 2001. إن الأبواغ التي يقل قياسها عن 5 میکرون صغيرة لدرجة يمكنها (إذا استنشقت) أن تصل إلى الطرق التنفسية السفلية وتسبب الجمرة الخبيثة الاستنشاقية.
إن حدوث الجمرة الخبيثة بشكل طبيعي نادر جداً في الولايات المتحدة. وإن الأشخاص المعرضين لخطر الجمرة الخبيثة هم بشكل رئيس أولئك الذين على تماس مع الحيوانات المصابة، ورغم حدوث الجمرة الخبيثة عند الحيوانات في الولايات المتحدة فإن هذه الطريقة في الانتقال نادرة. كذلك فإن موظفي المخابر وغيرهم من الأشخاص الذين على تماس مع أبواغ العصية الجمرية قد يكونون معرضين لزيادة خطر الإصابة على الرغم من أنه لم يسجل سوی حالتين من الجمرة الخبيثة المرافقة للمخبر (كانت كلتاهما جمرة خبيثة استنشاقية).
في الماضي كان من الممكن حدوث الإصابة عند الأشخاص الذين يتعاملون مع صوف الحيوانات المصابة أو شعرها أو جلودها أو عظامها. لكن التحسينات التي حدثت على الزراعة الحيوانية animal husbandry والشروط الصارمة المفروضة على استيراد منتجات الحيوانات جعلت هذا المصدر من الخمج نادراً جداً.
النموذج الفصلي
يمكن أن تحدث الجمرة الخبيثة على مدار السنة، بينما تحدث الحالات المرتبطة بالحيوانات بشكل رئيس في الربيع والصيف.
السراية
إن الأشخاص المصابين بالجمرة الخبيثة الاستنشاقية غير معديين. ورغم تسجيل حالات انتقال للجمرة الخبيثة الجلدية من شخص لآخر فإن ذلك نادر جداً.
الاتجاهات العامة
أكثر ما تحدث الجمرة الخبيثة عند الحيوانات العاشبة التي تصاب عن طريق التهام الأبواغ من التربة أو استنشاقها. أما إصابة الإنسان بشكل طبيعي فتحدث بعد التماس مع الحيوانات المصابة بالجمرة الخبيثة أو مع منتجاتها الملوثة.
يصعب تقدير نسبة الحدوث الحقيقية للجمرة الخبيثة عند الإنسان في العالم؛ نظرا لأن التبليغ عن حالات الجمرة الخبيثة غير موثوق به. وقد حصل أكبر وباء بشري بالجمرة الخبيثة حديثة في زيمبابوي خلال الفترة بين عامي 1978- 1980، حيث حدثت 9.445 حالة، من ضمنها 141 حالة وفاة (1.5 ٪).
أما في الولايات المتحدة فقد انخفضت نسبة الحدوث السنوية للجمرة الخبيثة عند الإنسان من 130 حالة في السنة تقريباً في مطلع القرن العشرين إلى أن انعدمت الحالات خلال الفترة ما بين عامي 1993 - 1999، وفي عام 2000 سجل حدوث حالة وحيدة من الجمرة الخبيثة الجلدية، وكانت مرتبطة مع جائحة للجمرة عند حيوانات المزارع في داكوتا الشمالية. بينما لم يسجل سوى 18 حالة جمرة خبيثة استنشاقية خلال القرن العشرين، حدث آخرها في عام 1976. أما الجمرة الخبيثة الهضمية فلم يسجل حدوثها في الولايات المتحدة.
باستثناء الحالة الوحيدة التي حدثت في عام 2000 فقد كانت كل الحالات التي حدثت في الولايات المتحدة منذ عام 1993 ناجمة عن التعرض لهجوم بيولوجي متعمد. ففي شهري تشرين الأول وتشرين الثاني من عام 2001 سجل حدوث 22 حالة (11 حالة استنشافية، 11 حالة جلدية). وكانت عصيات الجمرة موضوعة في مغلفين على الأقل، وقد أرسلا عبر بريد الولايات المتحدة. تعرضت معظم الحالات للخمج في مرافق الفرز البريدي أو أنها كانت على تماس مباشر مع المغلف الملوث. إن مصدر عصيات الجمرة المستخدمة في هذه الهجمات غير معروف.
تعريف الحالة
تعرف حالة الجمرة الخبيثة المؤكدة case بأنها حالة تتوافق سريرياً مع المرض الجلدي أو التنفسي أو الهضمي، وتكون مؤكدة مخبرياً بعزل العصية الجمرية من النسيج أو المكان المصاب أو بوجود دليل مخبري آخر على الخمج بالعصية الجمرية بناء على فحصين مخبريين داعمين على الأقل. أما حالة الجمرة الخبيثة المشتبهة فهي حالة تتوافق سريرياً مع المرض لكن بدون عزل للعصية الجمرية وبدون وجود فحص بدیل. لكن يوجد دليل مخبري على العصية الجمرية بناء على فحص مخبري داعم وحيد وهي حالة تتوافق سريرياً مع الجمرة الخبيثة ومرتبطة وبائياً مع تعرض بيئي مؤکد. لكن لايوجد دليل مخبري يؤكد الخمج بالعصية الجمرية. يجب تبليغ قسم الصحة المحلي أو وزارة الصحة مباشرة عن أي شخص يشتبه بإصابته بأي نمط من الجمرة الخبيثة.
لقاح الجمرة الخبيثة
نجح لويس باستور بإضعاف العصية الجمرية وإنتاج أول لقاح جرثومي حي مضعف للاستخدام عند الحيوانات في عام 1881. وفي عام 1939 تم تطوير لقاح حي محسن يحتوي عصيات جمرة غير ممحفظة وعديمة الفوعة (لقاح ستيرن Stern). واستعمل عند المواشي، وقد استمر استعماله كلقاح بيطري رئيس في نصف الكرة الأرضية الغربي. ترافق استعمال لقاحات المواشي مع حدوث وفيات عرضية عند الحيوانات، لذا اعتبرت اللقاحات الحية غير مناسبة للبشر.
في بدايات القرن العشرين تمت دراسة رشاحات عصيات جمرة مزروعة بشكل اصطناعي من حيث إمكانية استعمالها كلقاحات. وفي عام 1954 تم تطوير أول لقاح رشاحة زرعية بشري، وقد استعمل الشب alum في هذا اللقاح كمادة مساعدة. زود هذا اللقاح القرود بالتحصين، وسبب ارتكاسات قليلة وتأثيرات جانبية قصيرة الأمد، وقد استخدم فقط في دراسة فعالية التلقيح ضد الجمرة الخبيثة عند الإنسان التي أجريت في الولايات المتحدة. وفي أواخر خمسينيات القرن الماضي تم تحسين اللقاح عن طريق انتقاء سلالة عصيات جمرية تنتج قسماً أكبر من المستضد الواقي وإنتاج أوساط خالية من البروتين واستعمال هيدروكسيد الألمنيوم كمادة مساعدة بدلاً من الشب. وفي عام 1970 تم ترخيص استعمال هذا اللقاح (لقاح الجمرة الممتز anthrax (AVA vaccine adsorbed في الولايات المتحدة.
خصائص اللقاح
إن لقاح الجمرة الخبيثة الممتز AVA هو اللقاح الوحيد ضد الجمرة الخبيثة الذي تم ترخيصه من قبل إدارة الأغذية والأدوية FDA في الولايات المتحدة. وهو محضر من رشاحة لا خلوية لمزرعة سلالة من عصيات الجمرة المولدة للذيفان toxigenic غير الممحفظة. لا يحتوي هذا اللقاح جراثیم ميتة أو حية، حيث تحتوي الرشاحة مزيجاً من منتجات خلوية إضافة إلى المكونات الذيفانية الثلاث LF , EF, PA
يمتز اللقاح بهيدروكسيد الألمنيوم كمادة مساعدة adjuvant، ويحتوي لقاح AVA على كمية لا تتجاوز 0.83 مغ من الألمنيوم في كل جرعة (0.5 مل)، كما يحتوي على 0.0025٪ من كلور البنزثونيوم benzethonium chloride كمادة حافظة و 0.0037٪ من الفورمالدهید formaldehyde وكمادة مثبتة.
استمناع اللقاح وفعاليته
إن المستضد الرئيس المسؤول عن تكوين المناعة هو المستضد الوالي PA، حيث يطور ما يقارب %83 من متلقي لقاح AVA أضدادا للبروتين PA قابلة للكشف بعد أسبوعين من إعطاء الجرعة الأولى، بينما تصل النسبة إلى 91٪ عند الملقحين الذين تلقوا جرعتين أو أكثر من اللقاح. ويحدث انقلاب مصلي عند ما يقارب 95% من الملقحين مع حدوث ارتفاع عيار الأضداد من نوع IgG) IgG anti - PA) إلى أربعة أضعاف بعد تلقي ثلاث جرعات من اللقاح. ومع ذلك فإن العلاقة الدقيقة بين عيار الأضداد (أو تركيزها) والتحصين ضد الخمج غير معروفة بشكل مؤكد.
أجريت تجربة سريرية محكمة واحدة لدراسة الجمرة الخبيثة عند الإنسان، وكان ذلك بين عامي 1955 - 1959، حيث أجريت التجربة عند عمال المطاحن باستخدام اللقاح المرسب بالشب لقاح يعتمد على PA، ويعتبر طليعة AVA المرخص حالياً). وتم في هذه الدراسة المحكمة إعطاء اللقاح إلى 379 عاملاً، بينما أعطي 414 عاملاً لقاحاً موهماً placebo، و ترك 340 عاملاً دون إعطائهم أي شيء. وقد أثبتت هذه الدراسة أن اللقاح فعال في الوقاية ضد الجمرة الخبيثة الجلدية والاستنشاقية معاً) في 5 ,92% من الحالات. حدثت خلال هذه الدراسة جائحة من الجمرة الخبيثة الاستنشاقية عند المشاركين. وبشكل عام حدثت 5 حالات من الجمرة الخبيثة الاستشاقية عند الأشخاص الذين تلقوا اللقاح الموهم أو الذين لم يتلقوا أي لقاح. بينما لم تحدث أية حالة عند الذين تلقوا لقاح الجمرة الخبيثة. لا تتوفر معلومات حول فعالية لقاح الجمرة الخبيثة عند الأشخاص الذين تقل أعمارهم عن 18 سنة أو الذين تزيد أعمارهم عن 65 سنة.
ظهرت الفعالية الواقية للقاح المرسب بالشب (الشكل المبكر من لقاح رشاحة الى PA) ولقاح AVA في العديد من الدراسات على الحيوانات من خلال استخدام مختلف طرق التعرض للأبواغ.
يعتقد أن الجمرة الخبيثة الاستنشاقية عند قرود المكاك (الريص Thesus) هي التمثيل الأفضل للمرض عند الإنسان، وقد لوحظ أن AVA يعطي وقاية لمدة تزيد عن 100 أسبوع بعد التحدي الرئوي بعصيات الجمرة. إن مدة المناعة الناجمة عن التلقيح ب AVA عند الإنسان غير معروفة وتقترح معطيات الدراسات على الحيوانات أن مدة الفعالية بعد جرعتين من اللقاح قد تصل إلى 1 - 2 سنة.
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
جدول التلقيح والاستعمال
تتكون سلسلة التلقيح الأولي ب AVA من ثلاث حقن تحت الجلد الأسابيع 0 ، 2 ، 4 ، يليها إعطاء جرعات أخرى في الأشهر 6 ، 12 ، 18، وتوصي الشركة الصانعة للقاح بإعطاء جرعة معززة سنوياً للمحافظة على المناعة. إن الأساس الذي بني عليه جدول التلقيح السابق الذكر (جرعة في الأسابيع 0 ، 2 ، 4 ، ثم في الأشهر 6 ، 12 ، 18 ، ثم جرعة معززة سنوياً) غير واضح جيداً.
وكما هو الحال في اللقاحات المرخصة الأخرى لا توجد معلومات تدل على أن زيادة الفواصل الزمنية بين الجرعات يؤثر بشكل سلبي على استمناع وسلامة اللقاح. كما تجدر الإشارة إلى أن انقطاع جدول التلقيح لا يتطلب إعادة البدء بسلسلة كاملة من لقاح الجمرة الخبيثة أو إعطاء جرعات إضافية.
نظراً لتعقد جدول التلقيح الأولي المؤلف من 6 جرعات وزيادة تواتر الارتكاسات الموضعية في أماكن الحقن، فقد أجريت دراسات من أجل تقييم استمناع جداول التلقيح التي يتم فيها إنقاص عدد الجرعات واستخدام الحقن العضلي بدلاً من الحقن تحت الجلد. وقد أشارت النتائج التمهيدية إلى أن الجداول التي تستعمل فيها جرعات أقل وبفواصل زمنية أطول وباستخدام الحقن العضلي بدلاً من الحقن تحت الجلد تنتج تراكيز مشابهة من أضداد ال PA. ومع ذلك لم توافق FDA حتى الآن على استعمال أي جدول بديل.
التلقيح قبل التعرض
يستطب التلقيح ب AVA بشكل روتيني قبل التعرض عند الأشخاص الذين يقومون بأعمال تتضمن إنتاج كميات أو تراكيز من مزارع العصيات الجمرية وكذلك الذين يقومون بنشاطات تكون إمكانية إنتاج الضبوب فيها مرتفعة. أما موظفو المخابر الذين يطبقون إجراءات المستوى الثاني من السلامة الحيوية النظامية standard biosafety level 2 practices أثناء التعامل الروتيني مع العينات السريرية فليسوا معرضين لزيادة خطر التعرض لأبواغ عصية الجمرة.
لقد انخفض خطر التعرض عند الأشخاص الذين يعملون على تماس مع جلود الحيوانات المستوردة أو فرائها أو مسحوق عظامها أو صوفها أو أشعارها، وذلك من خلال تعديل المعايير الصناعية ووضع قيود على الاستيراد. لذا فلا يوصى بالتلقيح الروتيني قبل التعرض لأفراد هذه المجموعة إلا عندما تكون هذه المعايير والقيود غير كافية؛ لمنع تعرضهم لأبواغ الجمرة الخبيثة. كذلك لا يوصى بالتلقيح الروتيني للأطباء البيطريين في الولايات المتحدة؛ نظراً لانخفاض نسبة الحدوث عند الحيوانات. ومع ذلك يمكن أن يستطب تلقيح الأطباء البيطريين وغيرهم من الأشخاص ذوي الخطورة العالية الذين يتعاملون مع الحيوانات التي يمكن أن تكون مصابة في المناطق التي يكون حدوث الجمرة الخبيثة فيها عالياً.
يمكن أن يستطب التلقيح قبل التعرض عند بعض موظفي الخدمة العسكرية وغيرهم من المجموعات التي يمكن أن تتعرض لإطلاق متعمد لعصيات الجمرة. بينما لا يوصی حالياً بالتلقيح قبل التعرض للعاملين في الدفاع المدني أو في شرطة النجدة أو في المهن الطبية.
التلقيح بعد التعرض
يطور حوالي 83٪ من الأشخاص الملقحين استجابات مناعية محرضة باللقاح بعد تلقيهم جرعتين من اللقاح، بينما ترتفع الأضداد إلى أربعة أضعاف عند أكثر من 95% من الأشخاص الملقحين بعد إعطائهم ثلاث جرعات من اللقاح. وعلى الرغم من أن العلاقة الدقيقة بين عیار الأضداد والتحصين ضد المرض غير واضحة فقد أكدت دراسات الجمع بين أنظمة اللقاحات بعد التعرض والمضادات الحيوية عند الرئيسيات من غير الإنسان أن جرعة واحدة أو اثنين من اللقاح كانت كافية لمنع تطور المرض عند إيقاف المضادات الحيوية.
لا توجد إلا معطيات قليلة تتعلق بفعالية لقاح AVA بعد التعرض. وتشير الدراسات على الرئيسيات غير الإنسان nonhuman primates إلى أن التلقيح بعد التعرض ليس واقياً لوحده. ومع ذلك فقد أشارت الدراسات إلى أن الجمع بين المضادات الحيوية والتلقيح بعد التعرض فعال في منع حدوث المرض عند الحيوانات بعد تعرضها لأبواغ العصيات الجمرية. لقد وافقت FDA على استعمال اللقاح الحالي في التلقيح قبل التعرض فقط. أما العدد الأمثل لجرعات اللقاح المستعملة في الوقاية ما بعد التعرض فغير معروف.
الارتكاسات الجانبية التالية للتلقيح
إن أشيع التأثيرات الجانبية التالية للتلقيح ب AVA هي الارتكاسات الموضعية، وقد حدثت أثاء إجراء دراسات التقويم evaluations ما قبل الترخيص للقاح كما يلي:
• الارتكاسات الموضعية الصغرى (ظهرت بشكل حمامی erythema ووذمة edema وجساوة induration أقل من 30 ملم) حدثت بنسبة 20 % من التلقيحات.
• الارتكاسات الموضعية المعتدلة (وذمة وجساوة بين 30 - 120 ملم) حدثت في 3٪ من التلقيحات.
• الارتكاسات الموضعية الشديدة (وذمة أو جساوة تزيد عن 120 ملم) حدثت في 1% من التلقيحات.
تتطور الارتكاسات الموضعية غالباً خلال 24 ساعة من التلقيح، وتتراجع خلال 48 ساعة. وتحدث العقيدات تحت الجلد في مكان الحقن في 30% - 50٪ من متلقي اللقاح، وتستمر أسابيع عديدة.
في عدة دراسات قامت بها وزارة الدفاع حدثت ارتكاسات جهازية (نوافض، آلام عضلية، دعث، غثيان) في 5% - 35٪ من متلقي اللقاح. وغالباً ما تكون الارتكاسات الجهازية خفيفة وعابرة، وتكون الحمى غير شائعة بعد استعمال AVA. أما الارتكاسات الشديدة (مثل الارتكاسات الأرجية) فهي نادرة.
لقد تم تقييم الارتكاسات الجانبية التالية للتلقيح بلقاح الجمرة الخبيثة من خلال عدة دراسات أجرتها وزارة الدفاع في سياق برنامج التلقيح الروتيني ضد الجمرة الخبيثة. وقد أظهرت إحدى هذه الدراسات أن 1.9٪ من متلقي اللقاح قد حدث لديهم تحدد في أداء العمل أو تم تكليفهم بمهام جزئية بسبب الارتكاسات الموضعية. كما سجل لدى 0.3٪ منهم تغيب عن العمل لأكثر من يوم واحد، وراجع 0.5٪ منهم العيادات الاستشارية للتقويم، وتطلب شخص واحد (0.02 %) دخول المشفى بسبب الارتكاس في مكان الحقن. سجل حدوث الارتكاسات الجانبية عند النساء أكثر من الذكور .
لم تسجل أية دراسة حدوث أمراض مزمنة (مثل السرطان أو العقم) بعد التلقيح بلقاح الجمرة الخبيثة. وقد لاحظ معهد الطب Institute of Medicine) IOM) عند تقييمه لسلامة لقاح الجمرة الخبيثة أن الدراسات المنشورة لم تسجل حدوث تأثيرات جانبية هامة ناجمة عن اللقاح، لكن هذه الدراسات اقتصرت على دراسات قصيرة المدة.
لقد خلصت إحدى دراسات المتابعة المنشورة التي أجريت على العاملين في المخابر في فورت ديتريك Fort Detrick في ماريلاند Maryland إلى أنه خلال فترة 25 سنة من متابعة التلقيح بلقاح الجمرة الخبيثة لم يطور العاملون أي مرض غير اعتيادي أو أعراض غير مفسرة مرافقة للتلقيح. ولم يجد معهد الطب أي دليل على أن الناس يواجهون خطراً كبيراً لحدوث ارتكاسات جانبية مهددة للحياة أو محدثة لعجز دائم مباشرة بعد تلقيهم لقاح AVA مقارنة مع عموم الناس، كذلك لم يجد دليلاً مقنعاً على أن الناس يواجهون خطراً كبيراً لتطوير تأثيرات صحية جانبية طويلة الأمد، رغم أن المعطيات المتعلقة بذلك محدودة (كما هو الحال في كل اللقاحات).
قامت CDC بإجراء استقصائين وبائيين حول المخاطر الصحية للجنود الذين شاركوا في [[حرب
الخليج]]، حيث تم فحص العلاقة الممكنة مع عوامل عديدة من بينها التلقيح ضد الجمرة الخبيثة . وكانت النتيجة أن الأدلة العلمية الحالية لا تدعم ترافق التلقيح ضد الجمرة الخبيثة مع أمراض حرب الخليج.
لا تتوفر معطيات تتعلق بسلامة لقاح الجمرة الخبيثة عند الأشخاص الذين تقل أعمارهم عن 18 سنة أو تزيد عن 65 سنة.
قد تحدث الارتكاسات الجانبية عند الأشخاص الذين يجب أن يستكملوا سلسلة التلقيح ضد الجمرة الخبيثة بسبب زيادة خطر تعرضهم للإصابة أو بسبب متطلبات العمل. وقد تم تطوير العديد من البروتوكولات لتدبير الارتكاسات الجانبية الموضعية والجهازية النوعية، لكن لم يتم تقويم هذه البروتوكولات بتجارب عشوائية.
مضادات الاستطباب والتحذيرات
كما هو الحال في كل اللقاحات يعتبر AVA مضاد استطباب للأشخاص الذين تعرضوا لارتكاس أرجي شديد (تأقي anaphylaxis) لأحد مكونات اللقاح أو بعد جرعة سابقة من AVA. كما يعتبر لقاح الجمرة الخبيثة مضاد استطباب عند الأشخاص الذين شفوا من الجمرة الخبيثة بسبب ملاحظة حدوث ارتكاسات جانبية أشد عند متلقي اللقاح الذين لديهم قصة إصابة بالجمرة الخبيثة مقارنة مع الذين لم يعطوا اللقاح.
يعتبر المرض الحاد المعتدل أو الشديد من محاذير precautions إعطاء اللقاح، ويجب أن يتم تأجيل التلقيح إلى ما بعد الشفاء، لأن ذلك يمنع تراكب التأثيرات الجانبية للقاح على المرض المستبطن، ويمنع أن تعزى مظاهر المرض المستبطن بشكل خاطئ للقاح. بينما يمكن أن يستعمل اللقاح عند الأشخاص المصابين بأمراض خفيفة حتى مع وجود الحمى الخفيفة.
أما بالنسبة لاستعمال لقاح الجمرة الخبيثة عند النساء الحوامل فلم تنشر بعد دراسات تتعلق بذلك، لذلك لم يرخص أو يوصى باستعمال اللقاح خلال الحمل. يجب تلقيح النساء الحوامل ضد الجمرة الخبيثة إذا كانت فوائد التلقيح المحتملة تفوق المخاطر الكامنة على الجنين.
لا توجد معطيات تقترح ازدیاد خطر التأثيرات الجانبية المرافقة لإعطاء لقاح الجمرة الخبيثة للنساء المرضعات أو للأطفال الذين يرضعون من أمهاتهم.
يمكن استعمال AVA عند الشخص المكبوت مناعياً immunostappressed عند الضرورة، لكن قد تكون الاستجابة للتلقيح أقل من المرجو.
اللقاح والتعامل معه
يجب أن يتم خزن AVA بدرجة حرارة بين 2 م - 28 (15 ف - 46 ° ف)، مع الانتباه لعدم تجميده. ويجب استشارة الشركة المصنعة إذا تعرض اللقاح لدرجة حرارة التجمد أو بقي لفترة طويلة في حرارة الغرفة.
الوقاية بالمضادات الحيوية بعد التعرض
وافقت FDA على استعمال البروكائين بنسلين والسيپروفلوكساسين والدوكسي سيكلين في معالجة الجمرة الخبيثة.
ورغم أن مقاومة العصيات الجمرية التي تحدث بشكل طبيعي للبنسلين نادرة، فقد سجل حدوث مثل هذه المقاومة. إن المضادات الحيوية فعالة ضد الأشكال المنتشة من عصية الجمرة، لكنها غير فعالة ضد الأشكال البوغية.
عندما يتم تعرض الرئيسيات من غير الإنسان لاستنشاق أبواغ العصية الجمرية فيمكن لهذه الأبواغ أن تبقى حية في النسج من دون إنتاش منه لعدة أشهر بعد استنشاقها. وهذه الظاهرة من تاخر إنتاش الأبواغ والتي تؤدي إلى تطاول دور الحضانة لم تلاحظ في طرق الخمج الأخرى غير الاستنشاق.
في إحدى الدراسات تم تعريض قرود المكاك أربعة أضعاف الجرعة المميتة LD50 من أبواغ الجمرة الخبيثة (جرعة الأبواغ التي تؤدي لموت 50% من الحيوانات المتعرضة)، وقد قدرت نسبة الأبواغ التي بقيت حية في نسيج الرئة لمدة 42 يوماً ب 15% - 20% ولمدة 50 يوماً ب 2% ولمدة 75 يوماً بأقل من 1%، كما تم كشف الأبواغ عند الحيوانات حتى بعد 100 يوم من التعرض.
لا تعرف مدة بقاء أبواغ الجمرة الخبيثة في نسيج الرئة عند الإنسان، ويعتقد أن الجرعة المميتة LD50 عند الإنسان مشابهة للجرعة عند الرئيسيات الأخرى. وعلى الأغلب تعتمد مدة بقاء الأبواغ على مقدار الجرعة المستنشقة. ويقترح دور الحضانة المتطاول الذي سجل في جائحة جمرة خبيثة استنشاقية في الاتحاد السوفييتي أن كميات الأبواغ القاتلة يمكن أن تبقى لأكثر من 43 يوماً بعد التعرض الأولي.
الوقاية بعد التعرض في حالة الاستنشاق
يوصى بالوقاية ما بعد التعرض بالمضادات الحيوية ضد العصية الجمرية بعد التعرض للضبوب الذي يحوي أبواغ عصية الجمرة. ويمكن أن يحدث مثل هذا التعرض في المخابر أو في حوادث الإرهاب البيولوجي. بينما لم يسجل حدوث جمرة خبيثة استنشاقية عند الإنسان نتيجة للتماس مع الجمرة الخبيثة التي تحدث بشكل طبيعي عند الحيوانات.
وافقت الى FDA على استعمال السيبروفلوكساسين والسوكسي سيكلين والبروكالين بنسيلين G في الوقاية عند الإصابة بالعصية الجمرية بطريق الاستنشاق. ونظراً للخوف من إمكانية مقاومة العصية الجمرية فيجب في البداية استعمال السيبروفلوكساسين أو الدوكسي سيكلين في الوقاية حتى يعرف التحسس الجرثومي. ويمكن تحويل الوقاية الكيماوية بالمضادات الحيوية إلى البنسلين VK أو الأموكسيسلين خاصة عند الأطفال عندما يعرف التحسس الجرثومي وتكون الجراثيم حساسة للبنسلين وكان بالإمكان الوصول إلى التراكيز المثبطة الصغرى minimum) MIC inhibitory concentrations) بالمعالجة الفموية.
يجب الاستمرار بالمعالجة بالمضادات الحيوية لمدة 60 يوماً على الأقل حال استعمالها منفردة؛ نظراً لإمكانية بقاء الأبواغ بعد التعرض للضبوب. أما في حال توفر اللقاح فيمكن إيقاف المضادات الحيوية بعد استعمال ثلاث جرعات من اللقاح وفق الجدول النظامي (الأسابيع 0 ، 2 ، 4). وعلى الرغم من أن نظام التلقيح القصير (3 جرعات كان فعالاً عندما استعمل مع المضادات الحيوية للوقاية بعد التعرض، فإن مدة التعصين بعد التلقيح غير معروفة). لذلك يمكن أن يتطلب الأمر اللجوء للتلقيح الإضافي عندما يحدث تعرض لاحق.
استخدام المضادات الحيوية للوقاية بعد التعرض الجلدي أو الهضمي
لم تجر حتى الآن أية دراسة محكمة على الحيوان أو الإنسان لتقويم استعمال المضادات الحيوية وحدها أو بمرافقة التلقيح بعد التعرض لعصيات الجمرة سواء عن طرق الجلد أو عن طريق الجهاز الهضمي.
يمكن حدوث التعرض الجلدي - ونادراً الهضمي - عند الإنسان بشكل تالٍ لجائحات الجمرة الخبيثة عند المواشي. وبسبب نقص المعلومات واعتماداً على الفيزيولوجيا المرضية pathophysiology وأطوار الحضانة المسجلة والمحاكمة السريرية للخبراء حالياً، فإن الوقاية بعد التعرض في هذه الحالات تكون بإعطاء المضادات الحيوية لمدة 7 - 14 يوماً. يمكن أن تشمل المضادات الحيوية السيبروفلوكساسين أو الأوفلوكساسين أو الدوكسي سيملين أو البنسلين أو الأموكسيسلين.
المصادر
- د. عماد محمد زوكار، د. محمد أحمد نوح: المرجع الشامل في اللقاحات. دار القدس للعلوم، الطبعة الأولى 2005.
المراجع
للاستزادة
- Abakar, Mahamat H.; Mahamat, Hassan H. (September 2012). "Properties and Antibiotic Susceptibility of Bacillus anthracis Isolates from Humans, Cattle and Tabanids, and Evaluation of Tabanid as Mechanical Vector of Anthrax in the Republic of Chad" (PDF). Jordan Journal of Biological Sciences. 5 (3): 203–208. S2CID 36932865.
- Edmonds, Jason; Lindquist, H. D. Alan; Sabol, Jonathan; Martinez, Kenneth; Shadomy, Sean; Cymet, Tyler; Emanuel, Peter (28 April 2016). "Multigeneration Cross-Contamination of Mail with Bacillus anthracis Spores". PLOS ONE. 11 (4): e0152225. Bibcode:2016PLoSO..1152225E. doi:10.1371/journal.pone.0152225. PMC 4849716. PMID 27123934.
- Sekhavati, Mohammad; Tadayon, Keyvan; Ghaderi, Rainak; Banihashemi, Reza; Jabbari, Ahmad Reza; Shokri, Gholamreza; Karimnasab, Nasim (2015). "'In-house' production of DNA size marker from a vaccinal Bacillus anthracis strain". Iranian Journal of Microbiology. 7 (1): 45–49. PMC 4670467. PMID 26644873.
- Roy, P. Roy; Rashid, M. M.; Ferdoush, M. J.; Dipti, M.; Chowdury, M. G. A.; Mostofa, M. G.; Roy, S. K.; Khan, Mahna; Hossain, M. M. (2013). "Biochemical and immunological characterization of anthrax spore vaccine in goat". Bangladesh Journal of Veterinary Medicine. 11 (2): 151–157. doi:10.3329/bjvm.v11i2.19140.
- Kusar, D.; Pate, M.; Hubad, B.; Avbersek, J.; Logar, K.; Lapanje, A.; Zrimec, A.; Ocepek, M. (2012). "Detection of Bacillus anthracis in the air, soil and animal tissue". Acta Veterinaria. 62 (1): 77–89. doi:10.2298/AVB1201077K.
وصلات خارجية
- Bacillus anthracis genomes and related information at PATRIC, a Bioinformatics Resource Center funded by NIAID
- Pathema-Bacillus Resource